유기화학을 공부하는 데 있어, 또한 원활한 의사소통을 위해 유기화합물의 명명법(Nomenclature)을 아는 것은 매우 중요하다.
이 글에서는 유기화합물 중 가장 기본적인 알케인(Alkane)과 자주 쓰이는 치환기의 명명법을 알아보도록 하자.
글 말미에는 명명을 연습해 볼 수 있는 몇 가지 문제도 수록해 두었으니 참고하면 도움이 될 것이다.
1. 곧은 사슬 알케인(Alkane)의 명명

알케인, 또는 알칸은 가장 기본적인 구조를 갖는 유기화합물이다. (알칸은 일본에서 넘어온 독일식 발음인데, 대한화학회의 화학 용어 개정안에 따르면 미국식 발음인 '알케인'으로 표기하는 걸 권장한다. 이 글에서도 미국식 표기를 따를 것이다)
알케인은 오직 탄소와 수소만으로 이루어져 있다. 이러한 화합물을 탄화수소(Hydrocarbon)라 부르며, 유기화합물의 기초 뼈대가 된다.
또한 알케인의 탄소와 수소는 모두 단일결합으로 이어져 있다. 이처럼 한 화합물에 오직 단일결합밖에 존재하지 않을 때, 그 화합물을 '포화되었다(Saturated)'라고 표현한다.
즉, 모든 탄화수소는 크게 포화 탄화수소(Saturated hydrocarbon)와 불포화 탄화수소(Unsaturated hydrocarbon)로 나눌 수 있다.

포화 탄화수소와 불포화 탄화수소는 다시 탄소 사슬의 구조에 따라 사슬 모양(Chain)과 고리 모양(Ring, Cyclic) 탄화수소로 나눌 수 있다. 여기서 불포화 탄화수소 중 고리 모양인 '방향족(Aromatic)'을 제외한 탄화수소를 지방족(Aliphatic) 탄화수소라 부른다. 지방족과 방향족을 기준으로 탄화수소의 분류를 다시 나누면 다음과 같다.

이번 글의 주요 논의는 지방족이자 포화 탄화수소인 알케인(Alkane)에 대해서다.
알케인도 다시 사슬 모양 알케인과 고리 모양 알케인으로 나눌 수 있는데, 일단은 사슬 모양 알케인을 먼저 생각해 보자.

알케인은 우선 사슬을 구성하는 탄소의 수에 따라 명명된다.
탄소의 개수에 따라 Meth-, Eth-, Prop-... 하는 접두사가 붙고, 그 화합물이 알케인이라면 -ane이라는 접미사가 붙는다. 즉, 탄소 한 개짜리 알케인은 메테인(Methane), 두 개짜리 알케인은 에테인(Ethane)... 하는 식이다.
탄소 수에 따라 접는 접두사는 아래 표와 같다.
| 탄소 개수 | 명칭 | 탄소 개수 | 명칭 | 탄소 개수 | 명칭 |
| 1 | Meth- | 20 | Icos- / Cos- | 10n + 1 | Un- / Hen- |
| 2 | Eth- | 30 | Triacont- | 10n + 2 | Do- |
| 3 | Prop- | 40 | Tetracont- | 10n + 3 | Tri- |
| 4 | But- | 50 | Pentacont- | 10n + 4 | Tetra- |
| 5 | Pent- | 60 | Hexacont- | 10n + 5 | Penta- |
| 6 | Hex- | 70 | Heptacont- | 10n + 6 | Hexa- |
| 7 | Hept- | 80 | Octacont- | 10n + 7 | Hepta- |
| 8 | Oct- | 90 | Nonacont- | 10n + 8 | Octa- |
| 9 | Non- | 10n + 9 | Nona- | ||
| 10 | Dec- |
예)
· 탄소가 8개인 알케인 : 옥테인(Octane)
· 탄소가 16개인 알케인 : 헥사데케인(Hexadecane)
· 탄소가 37개인 알케인 : 헵타트리아콘테인(Heptatriacontane)
일반적으로 탄소 수가 10개를 넘어가는 알케인은 다루지 않으므로, 10까지의 접두사를 알아두는 것 정도면 충분하다.
2. 사슬 알케인의 구조

탄소 수가 1~3개인 메테인(Methane), 에테인(Ethane), 프로페인(Propane)의 구조식과 화학식, 분자 모형이다.
일반적인 사슬 알케인의 분자식은 CnH2n+2이다. 곧은 사슬 알케인에서, 이는 각각의 탄소가 2개의 수소와 공유결합을 하고, 양 끝의 탄소가 각각 한 개의 수소와 더 결합을 한다고 생각하면 편하다.
메테인부터 프로페인까지는 하나의 분자식에서 가능한 분자 구조가 하나뿐이다. 하지만 탄소 수가 4개인 뷰테인(Butane)부터는 상황이 달라진다.

뷰테인은 곧은 사슬 구조와 가지 구조, 두 가지 형태를 가질 수 있다. 이들은 화학식은 같으나 다른 구조를 가져 서로 다른 물리, 화학적 특징을 갖게 되는데, 이러한 화합물을 이성질체(Isomer), 그중에서도 특히 구조 이성질체(Structural isomer, Constitutional isomer)라 부른다. (다른 이성질체에 대해서는 나중에 자세히 다루도록 하자)
뷰테인에서 곧은 사슬 구조의 뷰테인을 n-뷰테인, 가지 구조의 뷰테인을 iso-뷰테인이라 부른다.
그럼 탄소가 5개인 펜테인은 어떻게 될까?
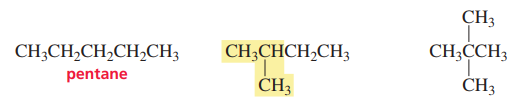
펜테인(Pentane)은 총 세 가지의 구조 이성질체가 있다. 곧은 사슬 구조(n형), iso 구조를 가진 형태, 그리고 사방으로 탄소가 뻗어나간 형태.
iso 구조란 iso 뷰테인에서 조금 더 확장되어, 탄소 사슬의 끝에 ㄱ자로 꺾인 구조를 의미한다고 생각하면 된다. 위 그림에서는 노란색으로 칠해진 부분이다.
사방으로 탄소가 뻗어나간 형태는 neo-라는 접두어를 붙여 neo-펜테인이라 부른다.
탄소가 6개일 때는?
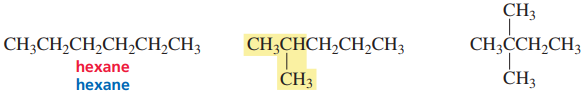
헥세인(Hexane)은 5개의 구조 이성질체를 갖는다. 그중 세 개는 앞서 언급한 명명법으로 이름 붙일 수 있다. 각각 n-헥세인, iso-헥세인, neo-헥세인(탄소가 사방으로 뻗어있으므로)이다.
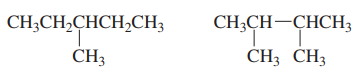
그럼 나머지 두 개의 이성질체는 어떻게 불러야 하는가? 접두사를 더 붙여야 하나?
이 문제점은 탄소 수가 늘어날수록 구조 이성질체의 수가 기하급수적으로 늘어난다는 점에서 기인한다. 탄소 수가 10개인 데케인은 75가지, 탄소 수가 15개인 펜타데케인은 4,347가지의 구조 이성질체를 가지므로, 접두어의 수를 늘리는 것으로는 해결할 수 없다.
그래서 화학자들은 이름에서 바로 그 화합물의 구조를 파악할 수 있는 명명법을 고안했고, 이를 체계적 명명법(Systematic nomenclature), 혹은 IUPAC 명명법(IUPAC nomenclature)이라 부른다.
이와 대비해서, Iso-, neo- 하는 명명법은 관용명(Common name)이라 한다. 탄소 수가 적은 유기화합물에서는 관용명이 더 효율적일 때가 있으므로 둘 다 알아두는 것이 중요하다.
그럼 이제 체계적 명명법을 알아볼 차례인 것 같지만... 그 전에, 우선 흔히 쓰이는 작용기의 명명법부터 알아보도록 하자.
3. 알킬의 명명
알케인에서 하나의 수소가 떨어져 나가 다른 화합물의 작용기로 작용할 때 이를 알킬(Alkyl) 치환체, 혹은 알킬기라 부르며, 보통 R-로 표기한다.
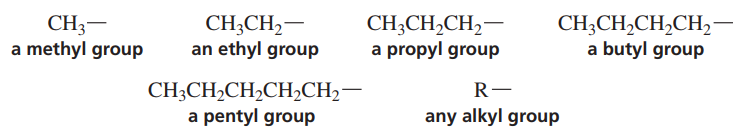
차례로 메틸기, 에틸기, 프로필기... 등으로 이름을 붙인다. 이들은 원래 메테인, 에테인, 프로페인... 등에서 유래되었다는 것을 기억하자.
알킬기는 어느 탄소에서 수소가 떨어져 나갔느냐에 따라 다른 구조를 가질 수 있다. 메테인은 하나의 탄소밖에 없으므로 하나의 구조밖에 갖지 못한다.
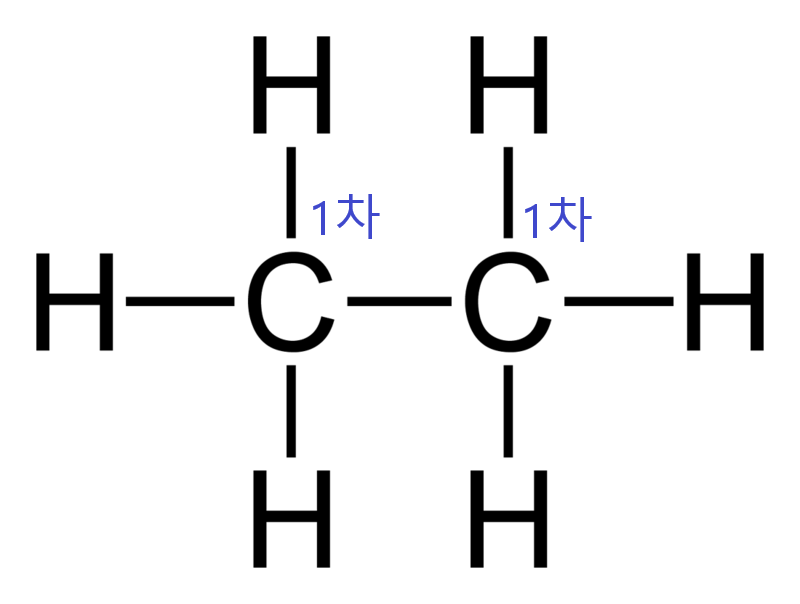
탄소를 구분하는 데 있어 각각의 탄소가 다른 몇 개의 탄소와 결합을 이루는가를 알아보는 것이 중요하다.
에테인의 경우 각각의 탄소가 서로 하나의 탄소랑만 결합을 이루고 있다. 이처럼 하나의 탄소와 결합을 이루는 탄소를 일차 탄소(Primary carbon)라 부른다. 즉, 에테인의 두 탄소는 모두 일차 탄소이고, 위치는 다르지만 근본적으로 같은 탄소다. 따라서, 둘 중 어느 탄소에서 수소기가 떨어져나오든 차이가 없다는 뜻이다. 그래서 에틸기는 이성질체가 존재하지 않는다.
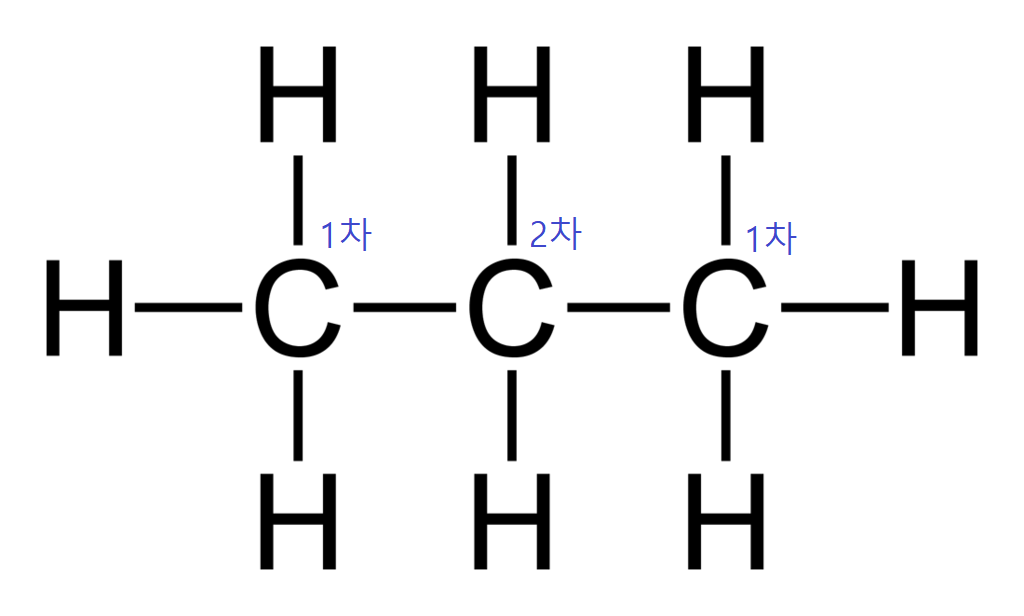
프로페인은 두 개의 일차 탄소와 한 개의 이차 탄소(Secondary carbon)를 갖는다. 양옆의 탄소와 가운데의 탄소는 다른 탄소이고, 따라서 둘 중 어디서 수소기가 떨어지느냐에 따라 다른 구조를 갖는 알킬기가 된다.
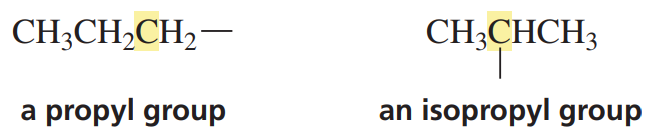
오른쪽의 프로필기에서 메틸기와 작용기의 위치를 바꾸면 앞서 언급했던 ㄱ자 구조를 갖지 않는가? 그래서 아이소프로필기(Isopropyl group)라는 이름을 붙인다. 알킬의 이름에는 흔히 관용명을 사용한다.
뷰테인을 생각해 보자. 뷰테인은 앞서 두 가지 이성질체가 존재했다. n-뷰테인과 iso-뷰테인. 각각의 뷰테인에서 유래되는 알킬기에는 어떤 것이 있을까?
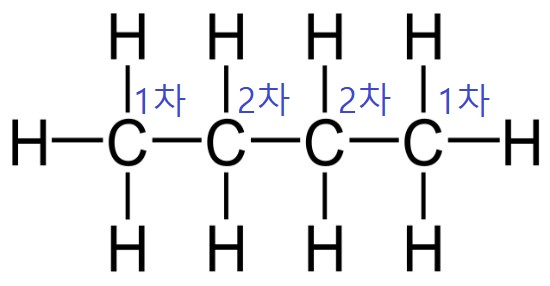
뷰테인은 일차 탄소와 이차 탄소를 각 두 개씩 갖는다. 일차 탄소에서 수소가 떨어져 나간 경우 일반적인 뷰틸기(Butyl group)가 된다. 그럼 이차 탄소에서 떨어져 나가면? Secondary에서 따온 접두어인 sec-을 붙여 sec-뷰틸기라 표기한다.
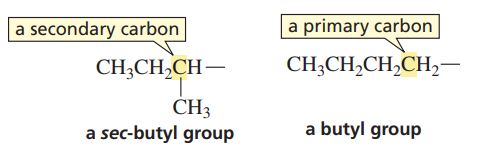
sec-뷰틸기는 iso 구조를 갖지 않는다. 딱 봐도 ㄱ자 모양의 구조가 없지 않나. 이차 탄소에서 수소기가 떨어져 나갔다는 것만 기억하자.
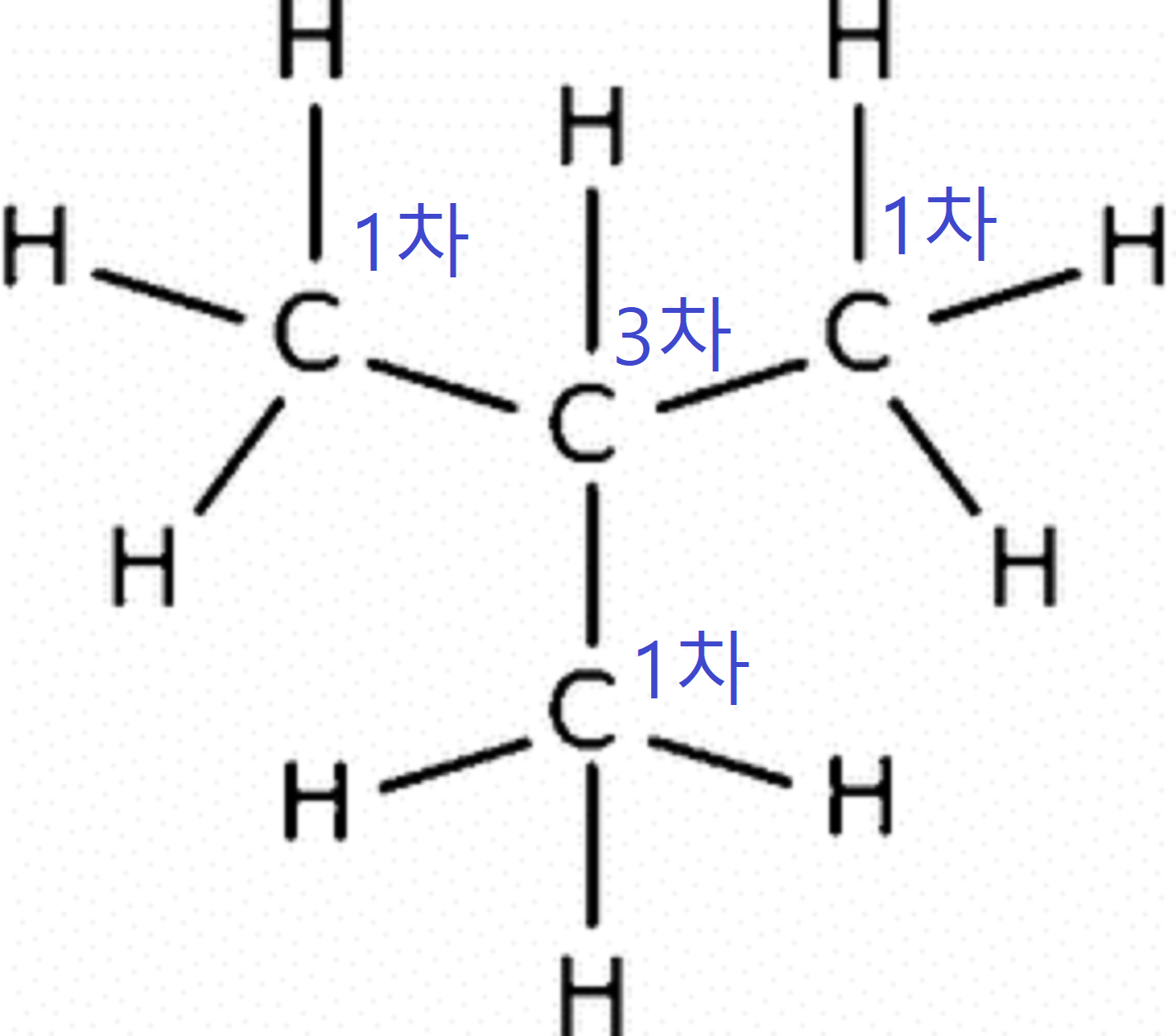
iso-뷰테인은 세 개의 일차 탄소와 한 개의 삼차 탄소(Tertiary carbon)를 갖는다. iso-뷰테인의 일차 탄소에서 수소가 떨어져나갔을 경우 아이소뷰틸기, 삼차 탄소에서 수소가 떨어져 나갔을 경우 Tertiary에서 따온 접두어인 tert-를 붙여 tert-뷰틸기라 부른다.

아이소뷰틸기에 ㄱ자 모양의 아이소 구조가 있음을 확인해 두자.
펜테인 이상으로 넘어가고서부터는 각각의 알킬기에 이름을 붙이는 과정이 너무 번거로워진다. 또한, 단순히 몇 차 탄소에서 수소가 떨어졌는지를 의미하는 sec-, tert- 등의 접두어가 기능하기 쉽지 않다. 따라서 곧은 사슬 알킬기와 iso 구조를 갖는 경우만 특별하게 기억해 두자.
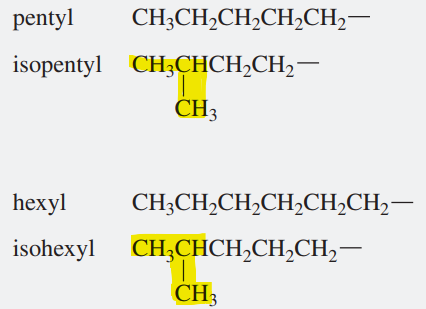
노란색으로 칠한 부분이 아이소 구조이다.
글이 길어진다.
명명체계를 숙지하는 것이 유기화학에서 하도 중요한 부분이다 보니 글에 많은 내용이 담기고 있는 것 같다. 다음 글에서는 자주 쓰이는 치환기와 제대로 된 다양한 화합물들의 명명법을 알아볼 것이다.
Q1. 탄소가 17개인 알케인은 몇 개의 수소를 갖는가?
Q2. 탄소가 7개인 알케인의 이름은 무엇이며, 몇 개의 구조 이성질체를 가질 것인가?
Q3. C5H12의 구조 이성질체 중 삼차 탄소가 1개인 경우가 존재하는가?
'유기화학' 카테고리의 다른 글
| [유기화학] 알케인의 명명 (Nomenclature of Alkane) - 2 (0) | 2023.10.10 |
|---|---|
| [유기화학] 산과 염기 (Acids and Bases) (0) | 2023.09.19 |
| [유기화학] 전자 구조와 결합 (Electronic Structure and Bonding) - 2 (0) | 2023.09.02 |
| [유기화학] 전자 구조와 결합 (Electronic Structure and Bonding) - 1 (0) | 2023.09.02 |