산-염기 반응은 유기화학에서 주요하게 다루는 반응 중 하나이다. 유기화합물과 다양한 치환기(Substituent group)의 거동을 설명하는 데 있어 산-염기의 원리가 자주 사용되기 때문이다. 이번 글에서는 산-염기의 정의와, 유기화학을 공부하는 데 필요한 몇 가지 산-염기의 원리에 대해 다뤄보도록 하자.
1. 산-염기의 정의

산-염기의 정의는 보통 세 가지로 구분된다.
아레니우스, 브뢴스테드-로우리, 루이스의 정의가 그것인데, 이들 정의를 각각 외우는 건 비효율적이기도 하거니와, 산-염기 반응의 '본질'을 이해하는 것과는 거리가 멀다.
조금 더 쉬운 비유를 들어 산-염기 반응이 무엇인지 이해해 보자.

'산도'란 산의 세기를 의미한다. 산도의 단위는 조금 이따 다시 다루도록 하고.
어떤 물질의 산도가 높다, 즉 산의 성질이 강하다는 것은, 그 물질이 '전자를 갖고자 하는 욕심이 많다.'는 것을 의미한다.
유기화학의 시작부터 전자 구조와 결합을 다룬 것에서 알 수 있듯, 전자(Electron)란 화학물질 사이에서는 꽤나 가치가 높은 '화폐'라 생각하면 편하다.
산도가 높은 물질은 산도가 낮은 물질로부터 전자를 뺏어온다.
산도가 낮은 물질은 본인보다 더 산도가 낮은 물질로부터 전자를 뺏어온다.
즉, 누가 전자를 뺏고 뺏기는지는 상대적이다. 그리고 이를 아는 게 산-염기 반응을 본질적으로 이해하기 위한 시작점이다.
그럼, 추상적으로 표현한 '산도'라는 개념을 수치화시켜보자.

모든 산 염기 반응은 수용액에서의 반응을 기준으로 나타낸다.
즉, 위 화학식에서 HA라는 물질은 사실 물과 반응해 하이드로늄 이온(H3O+)을 형성하는 것이다. 하지만 모든 반응에서 물을 작성하기 번거로우므로, 일반적으로 물을 생략한, 위와 같은 화학식으로 나타낸다.
위 반응식에서, HA의 산도란, A가 수소로부터 전자를 얼마나 잘 뺏어오느냐를 의미한다.

이 반응을 대략적인 모식도로 나타내면 다음과 같다. A는 수소로부터 전자를 뺏어버리고, HA는 H+와 A-로 분리된다.
즉, HA의 산도는 반응 후 분리된 H+와 A-의 농도를 측정함으로써 얻어낼 수 있다.

이를 수치로 표현하면, 다음과 같이 계산할 수 있다. [X]는 X의 몰농도를 뜻한다.
그리고 여기서 계산된 Ka를 산 해리 상수(Acid dissociation constant)라 부른다.
산 해리 상수는 보통 10의 거듭제곱 형태가 곱해진 매우 크거나 작은 값을 갖는데, 이를 조금 더 직관적으로 알아보기 쉽게 바꾸면 다음과 같다.

pKa의 값은 산 해리 상수의 값에 음의 로그를 취했기 때문에, 값이 작을수록 산도가 높아지게 된다. 일상적으로 사용하는 pH, 혹은 9등급제를 떠올리면 된다.
그런데 우리는 일상적으로 쓰는 산의 세기를 이미 알고 있다. pH이다. pH와 pKa는 무엇이 다를까?
pKa는 물질의 성질이다. 예를 들어, HCl(염산)의 pKa는 고정된 값, -7로 정의(Definition)되어있다.
반면, pH는 그 용액에 순전히 H+가 얼마나 녹아있냐를 측정한 값이다. 즉, 같은 산을 용해한 용액이더라도, 산의 농도가 얼마인지에 따라 값이 달라질 수 있다. 예를 들면 1 M HCl 용액과 0.1 M HCl 용액의 pH는 다르다.
pKa를 앞으로 편의상 '산도', 혹은 '산의 세기'라 부르도록 하자. 산의 세기가 강하다는 것은, 그만큼 pKa 값은 작다는 것이다. 이를 조금 비유적으로 표현하자면, 산의 세기가 높을수록 수소를 더더욱 내보내고 싶어 한다.
이쯤 되면 궁금한 점이 하나 있을 것이다. 그럼 염기는? 지금까지 실컷 산에 대한 이야기만 하지 않았나?
염기에게는 슬픈 이야기지만, 염기는 빛과 그림자로 치면 그림자 같은 친구다. 즉, '산'의 정의에 따른 부차적인 성질로 취급한다.

두 종의 물질이 반응할 때, 산의 세기가 상대적으로 강한 물질을 산(Acid), 산의 세기가 상대적으로 약한 물질을 염기(Base)라 정의하는 것이다.
즉, 어떤 물질이든, 반응하는 물질이 무엇이냐에 따라 산으로도, 염기로서도 기능할 수 있는 것이다.
그리고 이러한 정의가 산-염기 반응의 보다 근본적인 정의이다.
2. 짝산과 짝염기

염산과 물의 반응으로 다시 돌아가보자.
염산은 물보다 산의 세기가 강하다. 그러므로 염산의 Cl은 H로부터 전자를 빼앗고, 본인이 Cl-의 형태를 유지하려고 한다.
염산으로부터 빠져나온 수소는 물과 결합해 하이드로늄 이온을 형성한다.
즉, 염산과 물의 산-염기 반응 결과로 염소 음이온(Cl-)과 하이드로늄 이온(H3O+)이 생성된다.
그런데 반응물의 입장에서 보자.
Cl-는 이미 전자를 뺏었으니까, 전자를 빼앗으려는 힘이 상대적으로 약해진다.
반면, 물의 경우, 하이드로늄 이온이 되며 받고 싶지도 않은 수소 이온을 받아버렸으므로, 다시 어디선가 전자를 뺏어오고 싶어진다.
화학반응은 항상 역반응을 수반하므로, 결과적으로 반응물 사이에서는 Cl-가 염기, H3O+가 산의 역할을 하게 되는 것이다.
정반응에서는 산이었던 HCl이 역반응에서는 Cl-이 되어 염기의 역할을 수행한다. 우리는 이때 정반응의 산과 연결된 염기, Cl-를 'HCl의 짝염기(Conjugate base)'라 부른다. 물의 경우도 마찬가지로, 반응물인 하이드로늄 이온을 정반응의 염기였던 '물의 짝산(Conjugate acid)'이라 부른다.
다만 짝산과 짝염기는 위에서 언급했던 산-염기의 정의와 완전히 부합하지는 않는다. 짝산과 짝염기 중 짝염기의 pKa 값이 더 낮을 수 있다.
그러므로, 짝산과 짝염기는 항상 정반응의 산-염기를 기준으로 고려되어야 한다는 점을 기억하자. pKa 값을 비교하여 짝산, 짝염기를 고르는 것이 아니다.
이런 거추장스러운 구분을 왜 해야 하는가? 여러 이유가 있지만, 가장 중요한 건 정반응의 산과 짝산의 세기를 비교해 반응의 방향을 예측할 수 있다는 것이다.
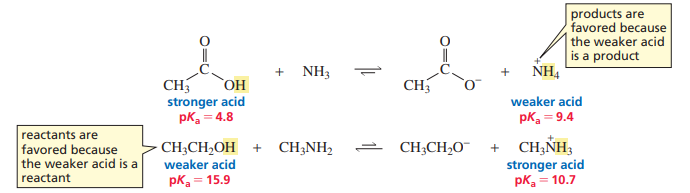
반응 양쪽의 산을 비교했을 때, 반응의 방향은 더 강한 산이 우세한 방향으로 향한다. 즉, 더 강한 산이 수소를 더 내놓고 싶어 한다.
정반응의 산이 더 강하면 정반응이 우세해진다.
반대로, 짝산의 세기가 더 강하면 역반응이 우세해진다.
짝산, 짝염기의 개념은 이처럼 아주 간단하게 산-염기 반응의 방향을 파악할 수 있게 해 준다.
3. pKa에 영향을 미치는 요인
다시 정리해 보자. 위에서 말이 길었지만, pKa 값은 다음의 두 가지 의미로 생각해 볼 수 있다.
① 전자를 뺏어가는 힘. pKa가 낮을수록 전자를 더 잘 뺏어간다.
② 수소 이온을 내보내려는 힘. pKa가 낮을 수록 수소 이온을 더 잘 내보낸다.
두 문장은 사실 같은 말이지만, pKa에 영향을 미치는 다양한 요인을 이해하는 데 있어 둘 모두를 알고 있는 건 큰 도움이 될 것이다.
1) 수소 이온이 더해질 때
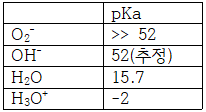
위 표는 산소에 수소 이온이 하나씩 더해질 때마다 pKa가 어떻게 변하는지를 나타낸 것이다.
수소가 없을 때부터, 수소가 하나씩 더해질 때마다 pKa 값은 낮아진다.
어떻게 보면 당연한 것이, 가지고 있는 수소가 많다면, 당연히 수소를 내보내기도 더 쉬워질 것이다.
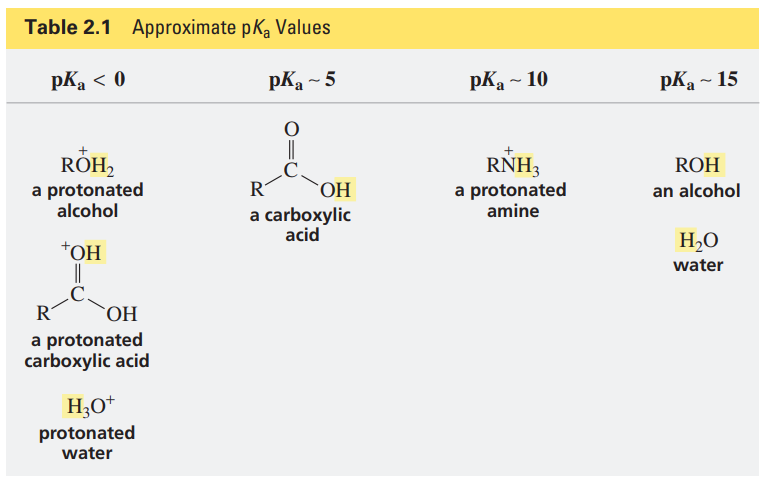
위 그림에서도, 수소 이온이 하나 더 많은(Protonated 된) 물질의 pKa 값이 더 낮다는 걸 볼 수 있다.
이 경향성을 이용해, 우리는 염기의 세기(Basicity)를 조금 다른 방법으로 정의할 수 있다.

각각 양성자화 메틸아민(Protonated methylamine), 양성자화 에틸아민(Protonated ethylamine)이라 불리는 화합물이다.
이들은 각각 메틸아민과 에틸아민의 짝산인데(수소를 하나 더 받았으므로), 짝산의 pKa만으로 원래 염기의 세기를 비교할 수 있을까?
둘의 pKa를 비교해 보면 양성자화 메틸아민의 pKa가 더 낮다는 걸 알 수 있다.
이는 즉, 양성자화 메틸아민은 수소를 내놓고 원래의 염기로 돌아가려는 경향이 양성자화 에틸아민보다 강하다는 걸 의미하고, 반대로 말하면, 메틸아민은 수소 이온을 받으려는 경향이 약하다는 말이기도 하다.
즉, 에틸아민이 더더욱 수소 이온을 더 잘 받아내며, 더 강한 염기가 된다.
결과적으로 짝산(혹은 양성자화된 물질)들의 염기의 세기를 비교하여 더 강한 쪽(pKa가 큰 쪽)이, 짝산이 되기 전에도 더 강한 염기라는 사실을 추론해 낼 수 있다.

Q1. 위 그림의 두 물질 중, 양성자화 되기 전 누가 더 강한 염기였을까?
2) 전기음성도(Electronegativites)

위 그림은 2주기 원소들을 전기음성도 크기대로 나열한 것이다.
원소들 각각과 수소의 결합물, CH4, NH3, H2O, HF의 pKa는 전기음성도의 영향을 받는다.
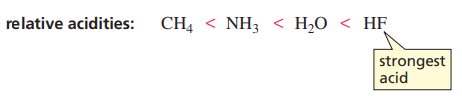
전기음성도(Electronegativites)는 쉽게 말해 '전자를 끌어당기는 힘'이다.
전자를 끌어당기는 힘이 강할수록 pKa가 낮다는 건 아까 이야기했었다.
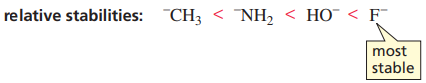
전자를 끌어당기는 힘이 강하다는 건, 그 원소가 음이온일 때 안정도가 높다는 말과도 같다.
즉, 전기음성도, pKa, 음이온의 안정성은 모두 연결되어 있다고 생각해 볼 수 있다.

Q2. 위 두 물질의 pKa 값을 대소비교해보자.
3) 혼성 오비탈
혼성오비탈이 pKa에 미치는 영향을 이야기하기 전, 두 가지 개념을 다시 짚고 넘어가자.
① 핵과 가까울수록 전자를 끌어당기는 힘은 세진다.
② 우리는 sp, sp2, sp3 혼성화를 배웠다.
s오비탈은 p오비탈에 비해 평균 거리가 핵과 더 가깝다. 이는 이들의 혼성화에도 적용된다.
s 오비탈과 핵과의 거리를 1, p 오비탈과 핵과의 거리를 2라 두면, sp 혼성 오비탈은 둘의 평균인 1.5 정도가 될 것이다.
마찬가지로 sp2는 1.666... sp3는 1.75 정도가 될 것이다. (예시이지 정확한 값은 아니다.)
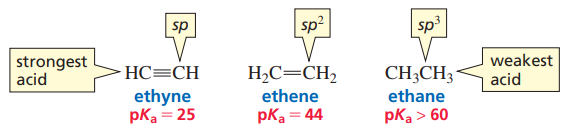
즉, 같은 탄소-수소로만 이뤄진 화합물이더라도, 그들의 결합이 어떤 혼성 오비탈을 이용하는지에 따라 pKa값이 달라질 수 있다. 실제로 sp 혼성화가 일어나는 에타인의 경우 정말 약한 산으로써 기능할 수 있을 정도로 pKa값이 낮아진다.
4) 원자 반지름
원자 반지름은 같은 족 내에서 주기가 높아질수록 커진다. 높은 주기의 원자는 더 큰 핵전하를 갖고, 이는 전자를 끌어당기는 힘이 더 강함을 의미한다.
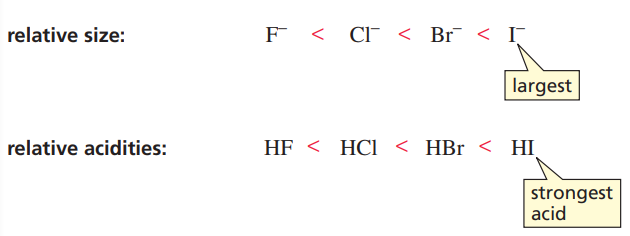
따라서, 17족 원소들 중 가장 원자반지름이 큰 아이오딘(I)이 수소와 결합한 HI이 가장 강한 산이며, 가장 낮은 pKa 값을 갖게 된다.
네 가지 요인을 정리하면 다음과 같다.
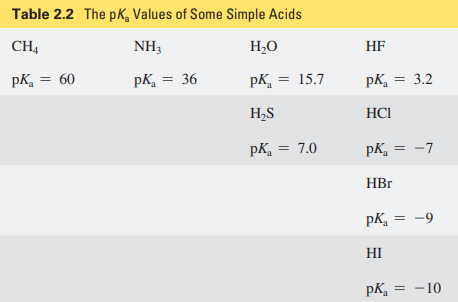
① 전자를 뺏어가는 힘. pKa가 낮을수록 전자를 더 잘 뺏어간다.
② 수소 이온을 내보내려는 힘. pKa가 낮을 수록 수소 이온을 더 잘 내보낸다.
이 두 줄이 pKa에 영향을 미치는 네 가지 요인을 관통하는 원리이니 꼭 기억해 두자.
4. 치환 효과(Substituents Affect)
전자를 끌어당기는 힘은 바로 옆 수소에게만 영향을 미치는 것이 아니다.
어떨 때는, 긴 화합물 끝에 달려 있는 원소(Cl, F와 같은)들이, 반대편 끝에 있는 수소에 영향을 주어 pKa를 더 끌어내릴 수 있다.
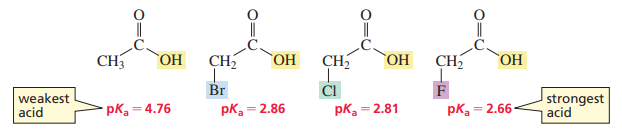
가장 왼쪽의 화합물에서, 수소 하나가 Br, Cl, F로 치환됨에 따라 pKa 값이 점점 낮아짐을 볼 수 있다.
이를 치환 효과(Substituents Affect)라 부르며, 치환 효과에 영향을 미치는 요인은 주로 앞서 다뤘던 전기음성도(Electronegativites)이다.
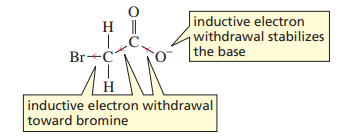
모식도로 보면, 맨 끝 수소의 전자를, 저 멀리 있는 브로민(Br)이 탄소 사슬을 따라 쭈욱 끌어오는 것이다.
이것이 브로민이 수소와 직접 결합한 것만큼 강하게 전자를 끌어당기지는 않겠지만, 어느 정도는 유의미한 영향을 준다.
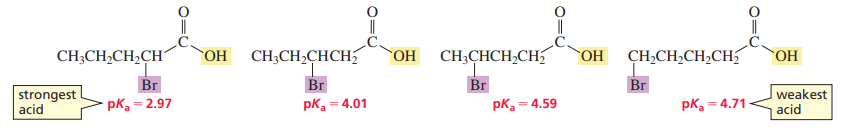
조금 더 긴 화합물의 경우, 치환기의 위치가 수소(산-염기 반응에서 떨어져 나가는 수소)와 멀리 떨어질수록 pKa는 높아진다. 즉, 산의 세기가 약해진다.
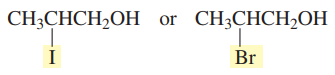
Q3. 두 화합물 중 pKa가 더 낮은 화합물은 무엇인가?
글이 길었다.
이번 글에서는 산-염기의 정의, 그리고 pKa에 영향을 끼치는 요인에 대해 다뤄보았다.
사실 이보다 조금 더 많은데, 추가적인 내용은 차후 필요한 때가 생기면 그때그때 설명하는 것이 나을 것 같다.
다음 글부터는 정말 유기화학의 시작이다.
가장 기본적인 알케인(Alkane)부터 알아보게 될 것이다.
'유기화학' 카테고리의 다른 글
| [유기화학] 알케인의 명명 (Nomenclature of Alkane) - 2 (0) | 2023.10.10 |
|---|---|
| [유기화학] 알케인의 명명 (Nomenclature of Alkane) - 1 (1) | 2023.09.29 |
| [유기화학] 전자 구조와 결합 (Electronic Structure and Bonding) - 2 (0) | 2023.09.02 |
| [유기화학] 전자 구조와 결합 (Electronic Structure and Bonding) - 1 (0) | 2023.09.02 |