이번 글에서는 생화학적 공통 반응과 생체 내 에너지 화폐로 사용되는 ATP의 기초적인 내용에 대해 이야기해보도록 하자.

대부분의 생체 반응은 다음의 다섯 가지 반응으로 정리할 수 있다.
1) 탄소 결합 형성 및 절단
2) 분자 내 전자의 재배열 (이성질화, 제거 반응을 포함한다.)
3) 유리라디칼 반응
4) 작용기의 전달 반응
5) 산화-환원 반응
각 반응에 대한 자세한 내용은 차후 대사 과정을 공부하며 나올 때 다시 살펴보도록 하고, 이번 글에서 자세하게 다룰 반응은 4) 작용기의 전달 반응, 그중에서도 특히 ATP의 인산기 전달 반응이다.
시작하기에 앞서 두 가지 기본적인 화학 원리에 대해 우선적으로 알아두자.
첫째, 공유결합은 균일(Homolytic)하거나 비균일(Heterolytic)하게 절단된다. 일반적으로 비균일 절단이 더 흔하다.
균일 절단은 두 개의 라디칼을 형성한다. 라디칼(Radical)은 홀전자를 가진 원자, 분자를 뜻한다.

비균일 절단은 전자쌍이 한쪽 원자로 치우쳐진다. 탄소 공유결합에서 비균일 절단은 불안정한 탄소 음이온과 탄소 양이온을 형성한다.

둘째. 많은 생화학 반응들은 친핵체(Nucleophile)와 친전자체(Electrophile)의 상호작용과 관련이 있다. 이들은 유기화학에서 쓰이는 용어인데, 쉽게 말해 다른 원자나 분자에게 전자쌍을 줄 수 있는 작용기를 친핵체, 전자쌍을 받아들일 수 있는 작용기를 친전자체라 생각하면 편하다.
친핵체는 전자쌍을 내놓을 수 있으므로 암모니아와 같은 '루이스 염기'라 생각해 볼 수 있다.

위 그림에서 빨간 점으로 표시된 것이 주고받는 전자쌍이다. 앞으로 '친핵 공격'이라는 말을 자주 사용할 텐데, 이는 친핵체의 전자쌍이 친전자체의 결합을 끊어내는, 쉽게 말해 전자쌍을 이용해 결합을 끊어내는 것이라 생각하면 좋다.
이제 본격적으로 ATP와 인산기 전달에 대해 알아보도록 하자.
APT는 아데닌과 리보스, 그리고 세 개의 인산기가 결합한 화합물이다. ATP에서 인산기가 하나 떨어져 나오면 ADP, ADP에서 인산기가 하나 더 떨어져 나오면 AMP라 부른다. 떨어져 나온 인산기 하나는 약자로 Pi라 쓴다.

ATP는 세포 내에서 물에 의해 가수분해되는데, 이때 ATP의 인산 결합들 중 하나가 친핵 공격을 받아 끊긴다. ATP 가수분해의 ΔG°는 -30.5 KJ/mol이다. 이는 큰 음의 값으로, ATP의 가수분해가 많은 에너지의 방출을 동반한다는 것을 뜻한다.
ATP가 이토록 큰 음의 자유에너지 값을 갖는 것은 인산기의 공명 구조와 관련이 있다. ATP 인산 세 개가 모두 붙어있을 때 각각의 인산기는 서로의 정전기적 반발력으로 인해 매우 불안정한 상태이고, 인산기 하나가 떨어져 나왔을 때 하나의 인산기는 공명 구조(Resonance)를 형성하여 안정해지기 때문이다.
즉, ATP는 불안정한 상태에서 안정적인 상태로 변하면서 에너지를 방출한다.

세포 내에서 ATP는 네 개의 산소 원자가 이온화된 ATP4-의 상태로 존재한다. ATP4-는 다시 세포 내에 흔히 존재하는 마그네슘 이온(Mg2+)와 결합해 보다 안정해진다.
ATP를 이용하는 효소 반응 대부분에서 실제 기질은 ATP가 아닌 안정화된 MgATP2-이다.

ATP의 ΔG°는 앞서 -30.5 KJ/mol이라 했다. 하지만 실제 세포 내의 ΔG(이를 흔히 ΔGP, 인산화 전위라 한다.)는 -30.5 보다 큰 음의 값으로 나타난다. 이는 ΔG에 영향을 주는 ATP, ADP, Pi 등의 농도가 세포 내에서 일정하지 않기 때문이다. 즉, 세포 내에서 ATP의 농도를 평형 상태 이상으로 유지하는 특수한 기작이 있다는 뜻이다.
만약 ATP의 농도가 평형 상태 이하라면, 이는 ATP의 양이 줄어들었다는 걸 뜻하기도 하지만, 뿐만 아니라 ATP 가수분해 반응의 ΔG 값이 -30.5보다 작은 음의 값을 갖게 되므로 ATP의 기능(가수분해되어 에너지를 공급하는 기능)이 유지될 수 없음을 의미한다.
ATP의 농도를 평형 상태 이상으로 유지해 ΔG를 보다 큰 음의 값으로 유지하는 기작은 매우 중요하다.
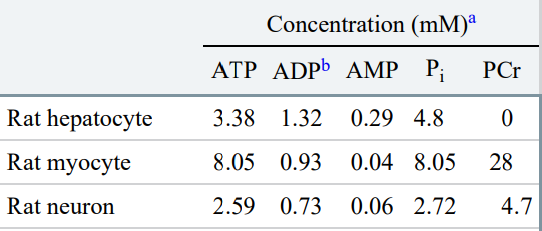
음의 자유에너지를 가진 인산화 화합물이 ATP만 있는 건 아니다. 이들은 각자 다양한 이유로 음의 생성물이 반응물에 비해 안정해 음의 자유에너지 값을 갖는다. 반응물을 안정화시키는 요인으로는 앞서 언급했던 공명 구조가 대표적이다.
ATP보다 큰 음의 자유에너지 값을 갖는 인산화 화합물로는 인산엔올피루브산, 1,3-이중인산글리세르산, 인산크레아틴 등이 있다. 이 중 인산엔올피루브산에 대해서는 알고 가는 것이 좋다.
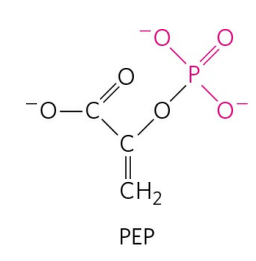
인산엔올피루브산(Phosphoenolpyruvate, PEP)은 피루브산(Pyruvate)에 인산기가 결합한 형태이다.
피루브산은 엔올형과 케토형의 두 가지 형태로 존재한다.
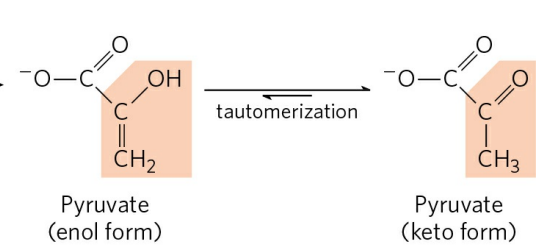
두 가지 형태 중 케토형이 엔올형보다 안정적인데, 인산기가 결합한 피루브산은 엔올형으로만 존재할 수 있다.
PEP가 가수분해되어 인산기가 떨어져 나와 피루브산이 되면, 피루브산은 케토형의 형태를 취할 수 있게 된다. 즉, 피루브산은 엔올형으로 존재할 수밖에 없는 PEP 보다 안정적이다. 이는 앞서 ATP 가수분해에서의 공명 구조처럼, PEP의 가수분해가 큰 음의 자유에너지 값을 갖는 이유를 설명해 준다.
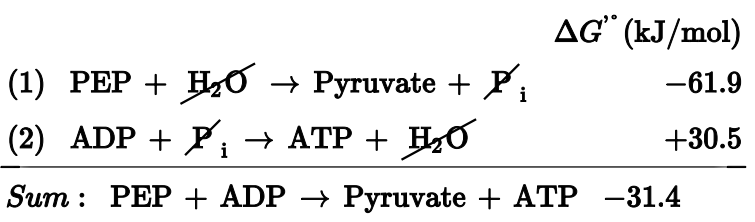
PEP의 ΔG°는 -61.9 KJ/mol로 ATP보다 크다. 밑에서 다루겠지만, PEP의 ΔG°가 매우 큰 음의 값이기 때문에, ATP를 재생시키는 데 PEP의 가수분해가 이용된다.
인산화 화합물이 아닌데도 큰 음의 자유에너지 값을 갖는 화합물이 있다. 앞으로 자주 접하게 될 '아세틸-CoA'가 대표적이다.
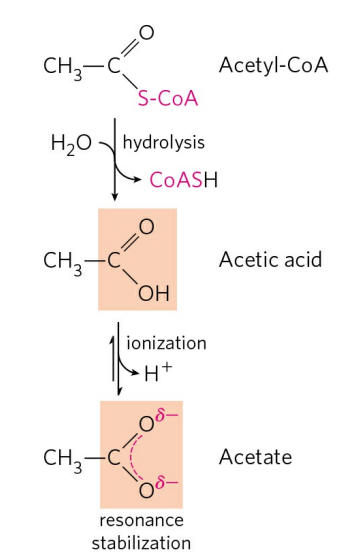
아세틸-CoA가 가수분해되어 만드는 아세테이트(Acetate)는 앞서 언급한 Pi의 경우처럼 공명 구조를 가져 안정화된다. 이는 ATP와 마찬가지로 아세틸-CoA가 큰 음의 자유에너지 값을 갖는 이유를 설명해 준다. 아세틸-CoA의 ΔG°는 -31.4 KJ/mol로 ATP의 ΔG°와 유사하다.
정리하자. ATP는 큰 음의 자유에너지를 갖는 화합물이다. 이는 Pi가 갖는 공명 구조의 안정성에서 온다. 실제 세포 내에서 ATP는 Mg2+와 결합한 상태로 존재하며, [ATP]가 높게 유지되기 때문에 실제 ATP의 ΔG는 ATP의 ΔG°보다 높게 측정된다. ATP 외에도 큰 음의 자유에너지 값을 갖는 화합물이 많이 존재하고, 대표적으로 PEP와 아세틸-CoA가 있다.
다시 ATP에 대한 이야기로 돌아와서, 그렇다면 ATP는 어떻게 에너지를 전달할까? 사실 ATP를 소모해 에너지를 이용하는 대부분의 생화학 반응은 ATP의 가수분해와 인산기 전달이 이뤄지는 숨겨진 반응이 존재한다.
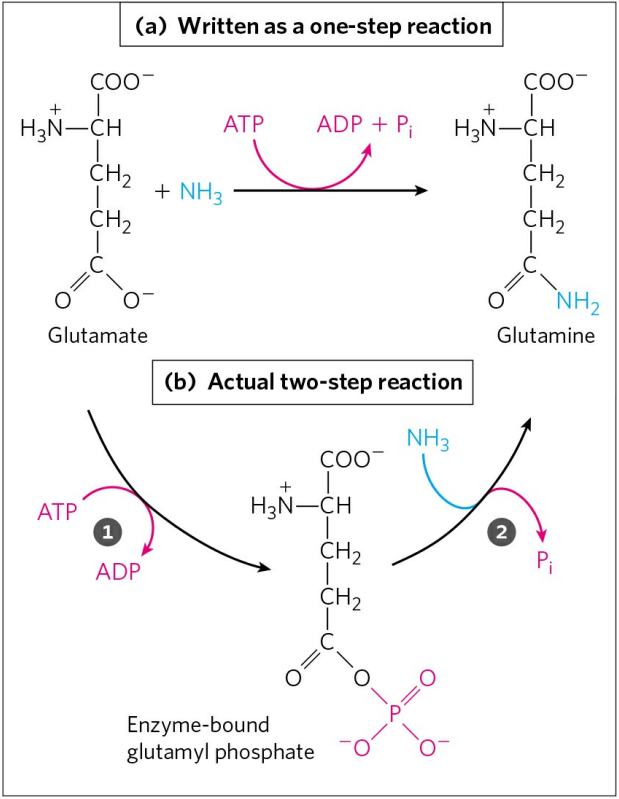
즉, ATP는 반응물에 자신의 인산기를 전달해 줌으로써 반응물을 활성화시키고, 이후에 인산기는 또 다른 반응물과 치환되며 방출된다. 쉽게 말해, ATP는 에너지를 저장하고 있는 건전지 같은 것이 아니라, 그 자체로 에너지인 셈이다.
ATP의 이런 인산기 전달 반응은 앞서 언급한 PEP에서도 일어난다. PEP는 ATP보다 자유에너지 절댓값이 더 크므로, ADP에 인산기를 전달해 ATP를 재생시킬 수 있다.
ATP는 비단 인산기만이 아니라, 세 가지 작용기를 전달해 줄 수 있다. ATP가 친핵 공격을 받는 위치에 따라 각각 인산기, 파이로인산기, 아데닐기를 전달한다.
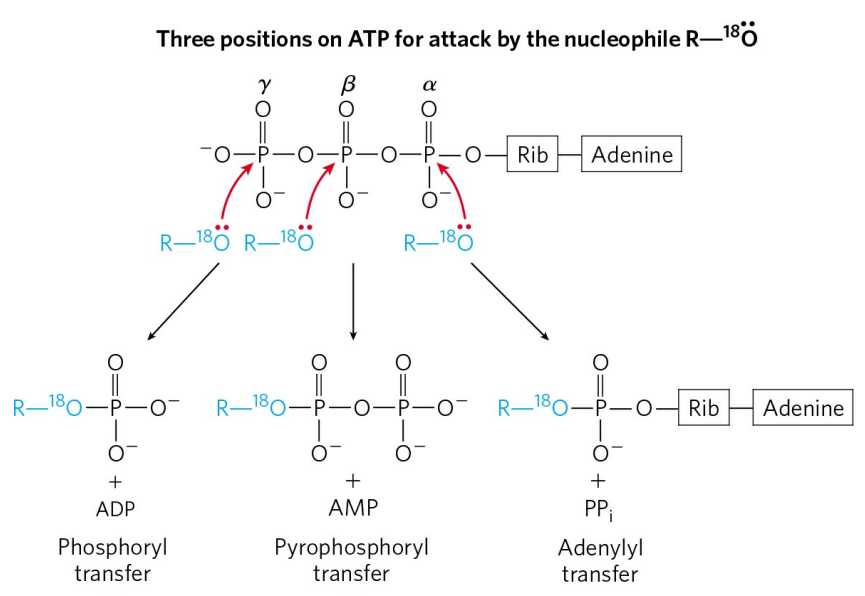
위 그림에서 γ 위치의 친핵 공격은 우리가 일반적으로 이야기하는 ATP의 인산기 전달 유형이다. ATP에서 인산기(-PO32-)가 전달되고, ADP가 떨어져 나온다.
β 위치의 친핵 공격은 파이로인산기(-PPi)를 전달해 주고, AMP가 떨어져 나온다.
α 위치의 친핵 공격은 따로 아데닐화(Adenylylation)라 한다. 이 반응은 아데닐기(-AMP)를 작용기로 건네주고 파이로인산이 떨어져 나오는데, 파이로인산은 다시 무기 탈파이로인산효소(Inorganicpyrophosphatase)에 의해 두 개의 무기 인산(Pi)으로 가수분해된다. 두 과정에서 각각 에너지가 방출되므로, 아데닐화 반응은 세 작용기 전달 반응 중 가장 많은 에너지를 방출한다.
여기까지 ATP에 대한 다양한 내용을 공부했다. 생체 내에서 에너지 화폐로 이용되는 ATP는 매우 중요하며, 앞으로 대사 과정을 공부할 때 지겹도록 보게 될 것이다. ATP의 작용기 전달, PEP, 아세틸-CoA 등 위 내용들을 확실히 익혀두면 공부할 때 많은 부분이 편해질 것이다. 꼭 기억해두자.
'생화학 > 생화학 (하)' 카테고리의 다른 글
| [생화학] 당분해 (Glycolysis) - 2 (0) | 2022.07.31 |
|---|---|
| [생화학] 당분해 (Glycolysis) - 1 (0) | 2022.07.31 |
| [생화학] 생물학적 산화-환원 반응 (Biological Oxidation-Reduction Reactions) (0) | 2022.07.30 |
| [생화학] 깁스 자유에너지 (Gibbs Free energy) (0) | 2022.07.29 |
| [생화학] 생체에너지학과 대사 (Bioenergetics and Metaboism) (0) | 2022.07.29 |