이번 글에서는 산화-환원, 특히 생체 내에서 일어나는 생물학적 산화-환원 반응에 대해 알아보도록 하자.

1. 산화-환원 반응 개요
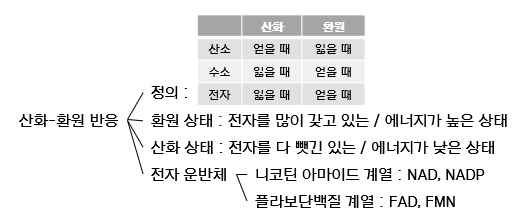
산화-환원 반응은 다음과 같이 정의된다.
| 산화 | 환원 | |
| 산소와의 결합 | 산소와 결합할 때 | 산소와 떨어질 때 |
| 수소의 이동 | 수소를 뺏길 때 | 수소를 얻을 때 |
| 전자의 이동 | 전자를 뺏길 때 | 전자를 얻을 때 |
이 중 가장 정확한 산화-환원 반응의 정의는 '전자의 이동'에 따른 정의이다.
모든 원소는 고유의 전자를 끌어당기는 힘, 전기 음성도를 갖고 있다. 생체 내 주요한 원소들의 전기 음성도 서열은 다음과 같다.
H < C < S < N < O ( 오른쪽으로 갈수록 전기 음성도가 커진다.)
예를 들어, CH4를 보면, 탄소가 수소보다 전기 음성도가 높으므로, 네 개의 공유 전자쌍은 모두 탄소 원자 쪽으로 이동한다. 이를 흔히 탄소 원자가 전자를 '소유한다'라고 표현한다.
한 분자가 전자를 주변 원자로부터 많이 뺏어온, 즉 전자를 많이 소유한 상태일 때 그 분자를 '환원된 상태'라 한다. 환원된 상태는 곧 그 분자가 많이 산화될 수 있음을 의미하고, 이는 다시 많은 에너지를 보유하고 있다는 걸 의미한다. 반대는 '산화된 상태'이다.
탄소 원자의 가장 환원된 상태는 CH4이다. 반대로, 탄소 원자의 가장 산화된 상태는 CO2이다. 즉, 모든 탄소 화합물의 연소 최종 산물(에너지를 모두 내놓은 상태)은 CO2가 된다.

생물학적 산화-환원 반응에서는 보통 전자의 이동에 더해 수소의 이동이 함께 일어난다. 전자를 뺏기는 산화는 탈수소화(Dehydrogenation)와 동일한 의미를 가질 때가 많다. 탈수소화를 촉매하는 탈수소효소(Dehydrogenase)는 대개 생체 내에서 산화 반응을 촉진한다.
2. 특별한 전자 운반체
포도당(C6H12O6)은 탄소 원자가 매우 환원된 상태이다. 즉, 큰 에너지를 가진 분자이다. 때문에 포도당은 여러 번의 산화를 거쳐 에너지를 방출하는데, 이 반응식은 다음과 같다.
$ C_6H_{12}O_6 + 6O_2 \rightarrow 6CO_2 + 6H_2O $
$ \Delta G˚ = -2,840 KJ/mol $
세포는 포도당을 한 번에 연소시켜 폭발적인 에너지를 얻는 것이 아닌, 여러 번의 반응을 거쳐 조금씩 에너지를 얻어낸다. 이 과정의 산화 반응이고, 산화 반응에서 포도당의 에너지는 전자로 방출된다. 이렇게 방출된 전자는 두 가지 특별한 전자 운반체로 이동한다.
1) NADH, NADPH
니코틴아마이드 아데닌 다이뉴클레오타이드(Nicotinamide adenine dinucleotide, NAD), 니코틴아마이드 아데닌 인산 다이뉴클레오타이드(Nicotinamide adenine dinucleotide phosphate, NADP)는 니코틴아마이드 고리와 아데닌 뉴클레오타이드가 결합한 화합물이다.

산화형인 NAD+(및 NADP+)는 기질로부터 두 분자의 수소 원자와 두 개의 전자를 가져온다. 이 중 하나의 수소 원자와 두 개의 전자는 NAD+(및 NADP+)와 결합해 NADH(및 NADPH)를 만들고, 남은 하나의 수소 원자는 수용액 중으로 방출된다.

NAD+(및 NADP+)라는 표기는 실제로 이 분자가 1가 양전하를 갖는다는 뜻이 아닌, 산화된 상태를 표기하는 것임을 유의하자. 때문에 간단히 NAD(및 NADP)로 표기해도 문제가 없다. NAD 전체 분자는 음전하를 갖는다.
대부분의 조직에서 NAD는 NADH보다 많이 존재한다. 때문에, NAD가 전자와 수소를 받아 NADH가 되는 반응이 잘 일어난다. 즉, NAD는 주로 기질을 산화시키는 데 이용된다. 탄소 화합물의 이화 반응은 대부분 산화 반응이므로 NAD가 관여한다.
반대로, 대부분의 조직에서 NADPH는 NADP보다 많이 존재한다. 때문에, NADPH가 전자와 수소를 내놓아 NADP가 되는 반응이 더 잘 일어난다. 즉, NADPH는 주로 기질을 환원시키는 데 이용된다. 탄소 화합물의 동화 반응은 대부분 환원 반응이므로 NADPH가 관여한다.
NAD와 NADP는 탈수소 효소의 보조인자(Cofactor)이다. 탈수소 효소와 이들은 느슨하게 연결되어 있어서, 한쪽 효소에서 전자를 얻어 NADH, NADPH가 되면, 이들은 다른 효소로 가 전자를 공여해주기도 한다.
또한, NAD와 NADH, NADP와 NADPH의 비율은 세포 에너지의 다양한 척도 중 하나이기도 하다. 이에 대한 이야기는 뒤에서 보다 자세히 다루도록 하자.
2) FADH2, FMNH2
플라보단백질(Flavoprotein)은 플라빈 모노뉴클레오타이드(Flavin mononucleotide, FMN), 플라빈 아데닌 다이뉴클레오타이드(Flavin adenine dinucleotide, FAD)를 보조효소로 사용하는 산화환원 효소이다.
NAD, NADP의 니코틴아마이드 고리처럼, FMN, FAD는 전자와 수소를 받아들이는 아이소알록싸신 고리(Isoalloxazine ring)를 갖고 있다.
이들은 NAD, NADP와는 다르게 한 개, 혹은 두 개의 전자와 수소 원자를 받을 수 있다. 한 개의 전자와 수소 원자를 받았을 경우 세미퀴논(Semiquinone) 구조가 되며, 간략하게 FADH·, FMNH·로 표기한다. 두 개의 전자와 수소 원자를 모두 받았을 경우 FADH2, FMNH2로 표기한다.

이들은 또 앞서 언급한 니코틴아마이드 계열 보조효소와는 다르게 플라보단백질에 아주 강하게 결합되어 있다. 이렇게 단백질에 강하게 결합된 보조효소를 보결단(Prosthetic group)이라 부른다. 플라보단백질과 이들의 기능은 뒷부분에서 보다 자세히 다루도록 하자.
여기까지 생물학적 산화-환원 반응에 대해 공부했다. 산화-환원 반응의 정의, 생물학적 산화-환원 반응과 함께 일어나는 탈수소 반응, 니코틴아마이드 계열 보조효소와 플라보단백질 보조효소는 앞으로 꾸준히 나오는 내용이다. 꼭 기억해두자.
'휴지통' 카테고리의 다른 글
| [생화학] 당분해 (Glycolysis) - 2 (0) | 2022.07.31 |
|---|---|
| [생화학] 당분해 (Glycolysis) - 1 (0) | 2022.07.31 |
| [생화학] 생화학적 공통 반응과 ATP (Common Biochemical Reactions and ATP) (2) | 2022.07.29 |
| [생화학] 깁스 자유에너지 (Gibbs Free energy) (0) | 2022.07.29 |
| [생화학] 생체에너지학과 대사 (Bioenergetics and Metaboism) (0) | 2022.07.29 |



