호기성 생물에서 에너지 대사의 궁극적 목표는 산화인산화(Oxidative Phosphorylation)다. 탄수화물, 지질, 아미노산의 분해 산물은 모두 시트르산 회로로 수렴되고, 시트르산 회로의 산물인 NADH와 FADH2는 다시 산화인산화를 거쳐 ATP를 생성한다. 비광합성 생명체에서 ATP는 대부분 산화인산화에 의해 공급된다. 진핵생물에서 산화인산화는 미토콘드리아 내막에 포함된 거대한 단백질 복합체에 의해 일어난다.

산화인산화의 기전은 세 가지 구성 요소를 필요로 한다. 이러한 기전은 화학삼투 이론(Chemiosmotic theory)에 기초한다.
① 일련의 막 결합 단백질 운반체를 통해 최종 전자 수용체(산소)로 전자를 전달한다.
② 전자의 흐름으로 방출된 자유 에너지는 양성자를 막사이공간으로 수송한다.
③ 양성자 수송으로 형성된 농도 기울기로 ATP를 합성한다.
이러한 기본 원리를 바탕으로 산화인산화에 대한 자세한 사항을 공부해보도록 하자.

1. 전자전달계 개요
산화인산화는 전자가 호흡 사슬(Respiratory chain)로 유입되면서 시작된다. 이 전자는 이화반응에서 NADH, FADH2로 전달된 것이다. 두 화합물의 구조와 이름에 대한 자세한 사항은 아래의 글을 참고하라.
[생화학] 생물학적 산화-환원 반응 (Biological Oxidation-Reduction Reactions)
이번 글에서는 산화-환원, 특히 생체 내에서 일어나는 생물학적 산화-환원 반응에 대해 알아보도록 하자. 1. 산화-환원 반응 개요 산화-환원 반응은 다음과 같이 정의된다. 산화 환원 산소와의
myw0rld.tistory.com
즉, 전자전달계의 시작점은 NADH, FADH2로부터 전자를 건네받는 것이다. 유입된 전자는 연속적으로 작용하는 일련의 전자 운반체를 거치며 조금씩 에너지를 잃어나가고, 궁극적으로 산소에 건네져 물(H2O)을 형성한다. 전자 운반체 사이에서는 3가지 유형의 전자 전달이 일어난다.
① 직접 전달 : Fe3+ ↔ Fe2+
② 수소 원자로의 전달 : H, 혹은 H+ + e-
③ 수소 음이온으로의 전달 : H-
흔히 산화환원 반응에서 환원 당량(Reducing equivalent)이라는 용어를 사용하는데, 이는 하나의 전자가 전달된 것을 표현하는 용어다. 예를 들어 ①과 ② 유형은 1개의 환원 당량, ③ 유형은 2개의 환원 당량을 갖는다고 말할 수 있다. 이는 전자의 운반 형태와 상관 없이 몇 개 분량의 전자가 이동하느냐를 표현하기 위함이다.
2. 전자 운반체
호흡 사슬 내에서 전자는 어떻게 운반되며 에너지를 잃는가? 호흡 사슬에서 전자를 운반하는 분자는 세 가지 유형이 존재한다.
1) 유비퀴논(Ubiquinone)
유비퀴논, 혹은 보조효소 Q(Coenzyme Q)라 불리는 분자는 아이소프레노이드(Isoprenoid) 가지를 갖는 퀴논 화합물이다. 퀴논은 벤젠 고리에서 수소가 산소로 치환된 화합물이다.

유비퀴논은 1개의 전자를 받아 세미퀴논 라디칼(Semizuinone radical, QH), 2개의 전자를 받아 유비퀴놀(Ubiqunol, QH2)을 형성한다. 때문에 유비퀴논은 1-전자전달(one-electron transfer)과 2-전자전달(two-electron transfer) 어느 쪽에도 관여할 수 있다.
유비퀴논은 또한 작은 소수성 분자이므로 미토콘드리아 내막을 자유롭게 이동할 수 있어 다른 전자 운반체들 사이에서 환원 당량을 전달할 수 있다. 또, 유비퀴논은 전자와 수소이온(양성자)를 동시에 운반할 수 있어 두 이동 반응의 중추적 역할을 수행한다.
2) 사이토크롬(Cytochrome)
사이토크롬은 헴(Heme) 보조단을 갖는 단백질이다. 헴 보조단은 내부에 철 이온이 함유된 포르피린 고리를 갖는 물질이다.

미토콘드리아는 a, b, c 세 부류의 사이토크롬을 함유한다. 각각의 사이토크롬은 헴 중심 철 원자를 이용해 전자를 운반한다. 사이토크롬 a와 b에서 헴은 단백질과 비공유결합으로 연결되어 있는 반면, 헴 c는 사이토크롬 단백질의 Cys 잔기와 공유결합으로 연결되어있다. 사이토크롬은 모두 미토콘드리아 내막의 내재 단백질이지만, 특별히 사이토크롬 c는 내막의 바깥(막사이 공간)과 정전기 상호작용을 통해 가역적으로 결합한다.
3) 철-황 단백질(Iron-sulfur protein)
철-황 단백질은 앞서 언급한 사이토크롬의 헴과 구조는 유사하나 다른 방식으로 철 원자를 묶어두는 단백질이다. 이들은 Cys 잔기와 황 원자를 이용해 철-황 중심부에 철을 가둬둔다.

철-황 단백질은 간단한 구조로부터 복잡한 구조에 이르기까지 다양한 종류가 있다. 철-황 단백질의 변형인 리에스크 철-황 단백질(Rieske iron-sulfur protein)은 Cys 대신 His 잔기를 사용한다.
모든 철-황 단백질은 1개의 환원 당량을 가지며, 이때 철 원자를 이용한다. 최소 8개의 철-황 단백질이 미토콘드리아 내 전자 전달 반응에 이용된다.
전자 운반체들의 전자 전달 서열은 실제 환원 전위 순서를 따른다. 환원 전위란 전자를 받으려는 경향성을 나타내고, 높을 수록 전자를 받으려는 경향성이 크다는 것을 의미한다. 호흡 사슬 내 다양한 전자 운반체의 서열 순서는 다음과 같다.
NADH → Q → 사이토크롬 b → 사이토크롬 c1 → 사이토크롬 c → 사이토크롬 a → 사이토크롬 a3 → O2
3. 전자 운반 복합체
호흡 사슬의 전자 운반체는 크게 네 개의 독특한 전자 운반 복합체(Electron carrier complex)로 분류할 수 있다.
1) 복합체 Ⅰ : NADH → 유비퀴논, NADH:유비퀴논 산화환원효소(NADH:ubiquinone oxidoreductase)
복합체 Ⅰ(Complex Ⅰ)은 FMN-플라보단백질과 8개 이상의 철-황 중심부를 포함하는, 45개의 폴리펩타이드로 구성된 거대 효소다. 복합체Ⅰ은 L자형의 구조를 가지며, 한쪽 팔은 미토콘드리아 내막에 박혀 있고, 다른 쪽 팔은 바탕질로 뻗어있다.

복합체 Ⅰ은 크게 두 개의 반응을 촉매한다.
① NADH에서 전자 2개를 유비퀴논으로 전달 : NADH + H+ + Q → NAD+ + QH2
② 양성자 4개를 바탕질에서 막사이공간으로 전달 : 4H+N → 4H+P
②에서 N은 바탕질, P는 막사이공간 쪽을 뜻한다. ② 과정은 특히 방향성이 중요하다. 미토콘드리아 막사이공간(Intermembrane space)은 높은 양성자 농도를 갖는데, 전자 전달 중 발생되는 에너지로 농도 차이를 거스르는 일종의 펌프질을 하는 것이다. 이렇게 펌프질된 양성자가 어떻게 이용되는지는 나중에 다루기로 하자.
전자를 전달받아 형성된 유비퀴놀(QH2)은 미토콘드리아 내막 인지질 이중충을 통과해 분산된다.
2) 복합체 Ⅱ : 석신산 → 유비퀴논, 석신산 탈수소효소(Succinate dehydrogenase)
시트르산 회로를 떠올리자. 시트르산 회로의 석신산 탈수소효소는 호흡 사슬의 복합체 Ⅱ(Complex Ⅱ)다. 복합체 Ⅱ는 A~D, 4개의 소단위를 갖는다. 그 중 C와 D는 내재 막 단백질이고, A와 B는 바탕질로 뻗어있다.
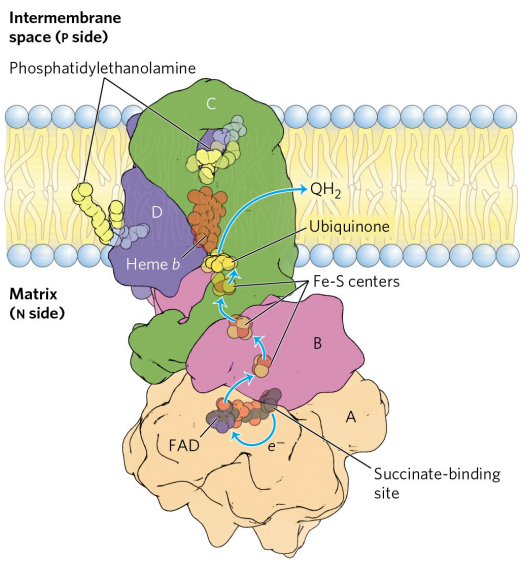
복합체 Ⅱ는 한가지 반응만을 촉매한다.
① 석신산에서 전자 2개를 유비퀴논으로 전달 : 석신산 + Q → 퓨마르산 + QH2
소단위 A와 B에 위치하는 석신산 결합자리에서 석신산은 FAD로 전자를 넘겨줘 FADH2를 형성한다. FADH2에서 방출된 전자는 3개의 철-황 중심부를 거쳐 Q로 전달되어 QH2를 형성한다.
복합체 Ⅱ는 또한 헴 b를 함유하고 있는데, 이는 전자전달의 직접 경로가 아닌, 계 밖으로의 전자 유출을 막는 역할을 한다. 헴 b가 없다면 활성 산소종에 의해 세포가 공격받을 수 있다.
3) 복합체 Ⅲ : 유비퀴논 → 사이토크롬 c, 사이토크롬 bc1 복합체(Cytochrome bc1 complex) 또는 유비퀴논:사이토크롬 c 산화환원효소(Ubiquinone:cytochorome c oxidoreductase)
복합체 Ⅲ(Complex Ⅲ)은 매우 큰 단백질 복합체다. 복합체 Ⅲ은 3개의 단백질로 구성된 복합체의 이합체다. 3개의 단백질은 각각 사이토크롬 b, 사이트크롬 c1, 리에스크 철-황 단백질이다.

복합체 Ⅲ은 크게 두 가지 반응을 촉매한다.
① 유비퀴논에서 전자 2개를 사이토크롬 c로 전달 : QH2 + 2 cyt c(산화형) → Q + 2 cyt c(환원형)
② 양성자 4개를 막사이공간으로 전달 : 2H+N + 2H+ → 4H+P
② 반응에서 2개의 양성자는 환원형 유비퀴논으로부터 유래된 것이다. 복합체 Ⅲ의 기전은 사실 조금 더 복잡하다. 이는 사이토크롬이 한 번에 오직 1개의 전자만을 운반할 수 있기 때문이다. 때문에 환원형 유비퀴논으로부터 유래된 2개의 전자는 하나씩 따로 다른 경로를 거쳐 사이토크롬으로 전달되어야 한다. 이를 설명하기 위해 Q 회로(Q cycle)을 이용한다.

한 분자의 QH2가 복합체 Ⅲ로 유입되는 것에서 시작해보자. 유입된 QH2는 산화되어 2개의 전자와 2개의 양성자, Q를 형성한다. Q는 인지질 이중층으로 분산되어 빠져나가고, 2개의 양성자는 막사이공간으로 전달된다. 2개의 전자는 각각 다른 경로를 거친다.
1개의 전자는 리에스크 철-황 중심(분홍색)을 지나 사이토크롬 c1(보라색)을 거쳐 사이토크롬 c로 전달된다. 나머지 1개의 전자는 사이토크롬 b(초록색)를 통해 유리 유비퀴논으로 전달되어 세미퀴논 라디칼을 형성한다.

다시 한 분자의 QH2가 복합체 Ⅲ로 유입되면 1단계와 같은 반응이 일어난다. Q가 분산되고, 2개의 양성자가 막사이공간으로 전달되며, 1개의 전자는 사이토크롬 c로 전달된다.
사이토크롬 b로 전달된 전자는 아까 생성했던 세미퀴논 라디칼(Q-)에 전달된다. 세미퀴논 라디칼은 미토콘드리아 내막에서 2개의 양성자를 받아 QH2를 형성한다. 생성된 QH2는 내막으로 분산된다.
두 단계를 거쳐 복합체 Ⅲ은 결과적으로 ①, ② 반응을 진행하게 되는 것이다.

Q 회로는 세미퀴논 라디칼을 형성함으로 때로는 위험할 수 있다. 세미퀴논 라디칼은 원래라면 빠르게 한번 더 환원되어 환원형 유비퀴논을 형성해야하지만, 그렇지 못할 경우 산소와 반응해 초과산화 유리 라디칼(O2-, ROS)을 형성하기도 한다. 이 반응은 다음의 두 조건에서 일어난다.
① 산소가 부족해 ATP를 합성하지 못하고, QH2를 빠르게 소모하지 못할 때.
② 바탕질의 NADH 농도가 유지되지 않고 높아질 때
이러한 상황에서 미토콘드리아는 높은 산화 스트레스를 갖는다. ROS에 의한 손상을 막기 위해 세포는 다양한 방어 기전을 갖고 있다; 초과산화물 불균등분해효소(Superoxide dismutase), 글루타싸이온 과산화효소(Glutathione peroxidase) 등
4) 복합체 Ⅳ : 사이토크롬 c → 산소, 사이토크롬 산화효소(Cytochrome oxidase)
복합체 Ⅳ는 13개의 소단위를 갖는 미토콘드리아 내막의 거대 효소다. 이 중 필수적인 소단위는 3개다. 복합체 Ⅳ는 구리를 함유하는 이핵 구리 중심부(Binuclear copper center)를 갖는다. 대표적인 독극물인 시안화물(청산가리)은 복합체 Ⅳ의 작용을 저해한다.

복합체 Ⅳ는 크게 두 가지 반응을 촉매한다.
① 사이토크롬 c에서 전자 2개를 산소로 전달 : 2 cyt c(환원형) + 1/2 O2 + 2H+N → 2 cyt c(산화형) + H2O
② 양성자 2개를 막사이공간으로 전달 : 2H+N → 2H+P

복합체 Ⅳ의 소단위 Ⅱ는 철-황 중심부와 유사하게 2개의 Cys 잔기와 결합한 2개의 구리 이온을 갖고 있다. 사이토크롬 c의 전자는 우선 소단위 Ⅱ의 구리 이온(CuA)으로 옮겨진다. 이후 소단위 Ⅰ에 위치한 헴 a로, 헴 a에서 헴 a3-CuB로, 최종적으로 산소 분자로 전달된다. 전자가 산소 분자로 전달되면 산소 분자는 바탕질로부터 양성자를 받아와 물을 형성한다. 2개의 전자가 복합체 Ⅳ에 유입될때마다 1분자의 물이 생성된다.
4개의 복합체는 서로 긴밀하게 연결되어 레스피라솜(Respirasome)이라 불리는 기능적 복합체를 형성한다. 때문에 전자 흐름은 전자 전달 복합체 사이에서 견고하게 보호된다.
5) 외부 경로
NADH, 석신산 외에도 호흡 사슬로 전자가 유입되는 여러 외부 경로가 있다.

트라이아실글리세롤은 산화되기 전 글리세롤과 지방산으로 분해된다. 글리세롤은 3-인산 글리세롤을 거쳐 산화되어 당분해 경로로 들어가는데, 이때 작용하는 3-인산 글리세롤 탈수소효소(Glycerol 3-phosphate dehydrogenase)는 복합체 Ⅱ와는 다른 FAD를 함유하는 플라보단백질이다. 3-인산 글리세롤 탈수소효소는 막사이공간 쪽으로 뻗어있다는 점을 기억해두자.
또한, β 산화의 첫 번째 단계에 작용하는 아실-CoA 탈수소효소 또한 플라보단백질이다. 아실-CoA 탈수소효소는 플라빈단백질(ETF, 리보플라빈을 함유하는 단백질)을 통해 최종적으로 Q를 환원시킨다.
피리미딘합성에 작용하는 다이하이드로오로트산 탈수소효소(Dihydroorotate dehydrogenase)는 미토콘드리아 막사이공간에 존재하며, FMN을 통해 Q를 환원시킨다. 이에 대한 자세한 사항은 피리미딘의 생합성을 공부할 때 다시 다루도록 하자.
6) 식물의 호흡 사슬
나중에 배우겠지만, 식물 미토콘드리아는 광호흡(Photorespiration)에 의한 손실을 메꾸기 위해 다음과 같은 반응을 수행한다.
$ 2 Gly + NAD^+ \rightarrow Ser + CO_2 + NH_3 + NADH + H^+ $
이 반응은 식물에서 항상 일어나는 반응이다. 결과적으로 NADH는 식물에서 필요량 이상으로 생성되고, 따라서 NAD+의 재생을 위해 식물 미토콘드리아는 NADH에서 직접 유비퀴논으로, 이후 바로 산소로 전달되는 특이한 호흡 사슬을 갖는다. 이때 전자의 에너지는 ATP를 합성하는 데 쓰이지 않고 열로 방출되는데, 이 열은 식물이 겨울을 나거나 악취를 낼 때 이용한다. 이 전자 전달계는 복합체 Ⅳ를 우회하므로 시안화물에 내성을 갖는다.
4. 양성자 기울기
1분자의 NADH는 호흡 사슬로 2개의 전자를 전달하고, 2개의 전자는 1분자의 물을 생성한다. 이 반응식은 다음과 같다.
$ NADH + H^+ + {1 \over 2}O_2 \rightarrow NAD^+ + H_2O $
이 반응의 표준 자유에너지는 -220 KJ/mol인데, 실제 세포 내에서 NADH의 농도는 표준 상태보다 훨씬 높으므로, NADH의 산화 반응은 매우 큰 에너지 방출 반응이 된다. (석신산의 전자 방출 반응도 NADH보다는 작지만 큰 에너지 방출 반응이다.)

이렇게 방출된 에너지는 호흡 사슬에서 막사이공간으로 양성자를 펌프질하는데 이용한다. 복합체 Ⅰ에서 4개, Ⅲ에서 4개, Ⅳ에서 2개로 총 10개의 양성자가 막사이공간으로 전달된다.
$ 10H^+_N \rightarrow 10H^+_P $
막사이공간으로 양성자가 전달되면 에너지는 양성자-구동력(Proton-motive force)으로 보존된다. 양성자-구동력은 두 가지 성분을 갖는다.
① 바탕질과 막사이공간 사이의 양성자 농도 차이 : 화학 전위 에너지(Chemical potential energy)
② 양성자가 막을 통과할 때 생기는 전하의 흐름 : 전기 전위 에너지(Electrical potential energy)
전기화학적 기울기에 의해 생긴 양성자-구동력은 양성자가 이를 해소하기 위해 움직일 때, 즉 기울기를 따라 양성자가 미토콘드리아 내막을 통과해 흐를 때 일을 할 수 있도록 만든다. 미토콘드리아, 엽록체, 호기성 세균 등에서 이 일은 ATP의 합성, 인산화다. ATP의 합성은 고도로 전문화된 ATP 생성효소(ATP synthase)가 담당한다.
ATP 생성효소는 어떻게 ATP를 합성하는가? 이에 대해서는 다음 글에서 다뤄보도록 하자.
'휴지통' 카테고리의 다른 글
| [생화학] 산화인산화 (Oxidative Phosphorylation) - 3 (0) | 2022.09.05 |
|---|---|
| [생화학] 산화인산화 (Oxidative Phosphorylation) - 2 (0) | 2022.09.03 |
| [생화학] 아미노산 분해 경로 (Pathways of Amino Acid Degradation) (0) | 2022.09.01 |
| [생화학] 요소 회로 (Urea cycle) (0) | 2022.09.01 |
| [생화학] 아미노기 대사 (Metabolism of Amino Groups) (0) | 2022.08.21 |



